Gemeten met: Ocean Optics Jaz spectrometer en een LED lichtbron van 312 nm.
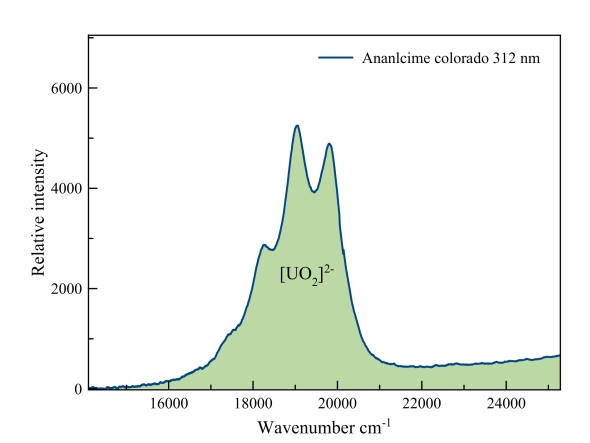
Analciem
De fingerprint van de uranyl-fluorescentie is overduidelijk.
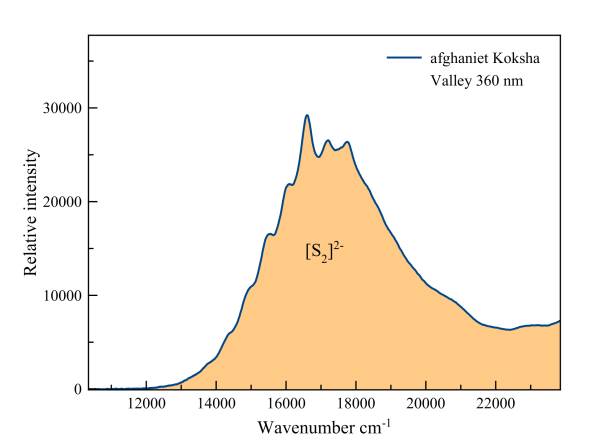
Afghaniet
Deze fluorescentie is "vibronisch", het gevolg van de vibratie van de twee zwavel-ionen rond het midden van de covalente binding die hen bindt. Met de verandering van de interatomaire afstand wordt ook een reeks mogelijke overgangen reëel. Elk van die overgangen uit zich als een "bult" op het spectrum.
Agrelliet + Albiet
Beweeg de muispijl over het spectrum om dat van albiet te zien.
De fluorescentie van agrelliet wordt beheerst door de emissies van driewaardig cerium, dysprosium en samarium. Tweewaardig mangaan levert ook een kleine bijdrage. Hoogstwaarschijnlijk zijn er nog een aantal andere zeldzame aarden actief maar die emissies verdinken in het geheel. Het leeuwenaandeel van de fluorescentie vindt plaats in het nabije UV.
De dieprode fluorescentie van albiet is voornamelijk gevolg van driewaardig ijzer dat aluminium vervangt. Mogelijk is ook wat tweewaardig europium aanwezig.
Zie ook Geonieuws jan. 2010.
Gemeten met: Ocean Optics Flame spectrometer, reflection/backscattering probe en een LED lichtbron van 360 nm.
Gemeten met: Ocean Optics Flame spectrometer, reflection/backscattering probe en een LED lichtbron van 255 nm.
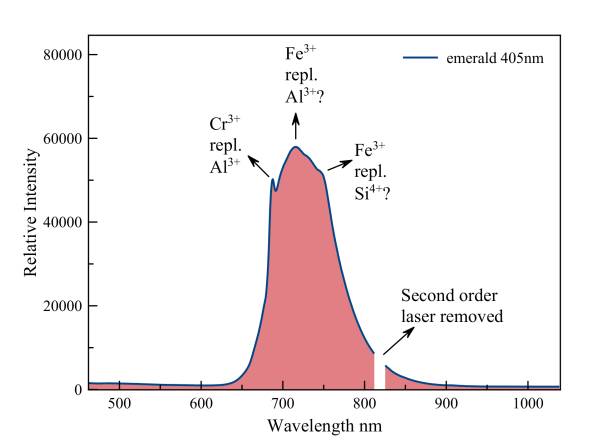
Beryl, var. Smaragd
De scherpe piek van fluorescerend chroom dat, aluminium vervangt, leunt aan tegen een veel sterkere emissie van driewaardig ijzer dat zowel aluminium als silicium kan vervangen. Het piekje van de tweede orde van de 405 nm laser werd verwijderd.
Gemeten met: Ocean Optics Jaz spectrometer, de backscattering/reflection probe en een diode laser van 405 nm.
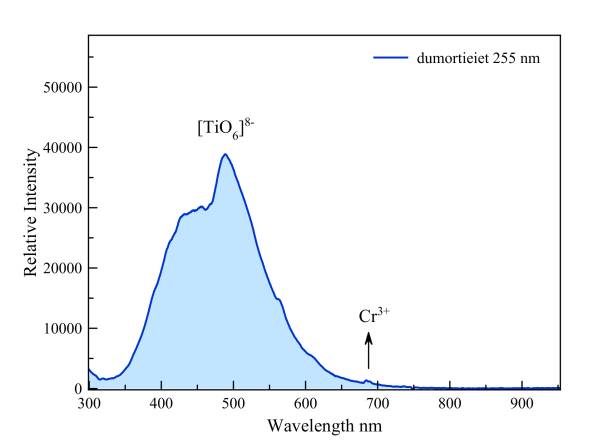
Dumortieriet
Volgens Gorobets is de blauwe fluorescentie onder korte golf UV te wijten aan vierwaardig titaan wat, als [TiO6]8-, dat aluminium vervangt (AlVI3+). Er is ook een emissie mogelijk in het rode gebied van het spectrum door driewaardig chroom dat ook Al3+ kan vervangen. Deze emissie wordt sterker geëxciteerd door laserlicht van 337 nm maar is onder korte golf UV toch nog juist zichtbaar bij 681 nm en 688 nm.
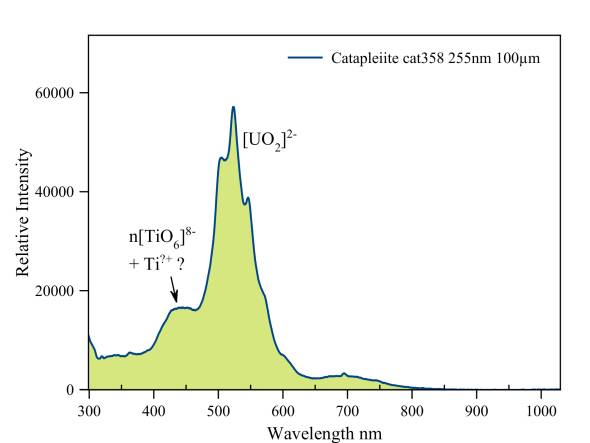
Catapleiiet
Dit specimen heeft een "dubbele" fluorescentie. Vooreerst is er de blauwe fluorescentie van drie- en vierwaardig titaan.
Ook het uranyl ion is aanwezig. Dat zorgt dan weer voor een groengele fluorescentie. De overheersende visuele indruk is een zwak groene fluorescentie.
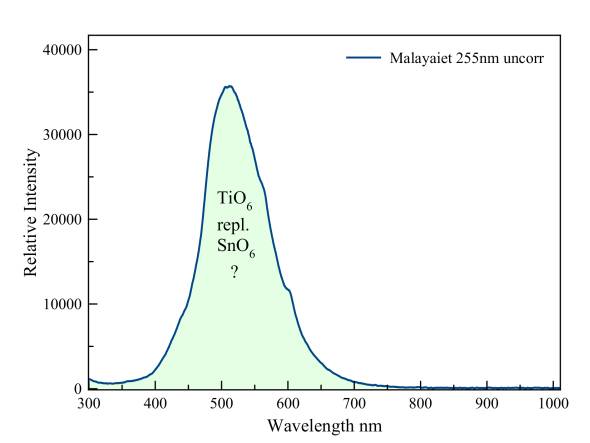
Malayaiet is de tin-homoloog van titaniet. Volgens Gorobets is de fluorescentie waarschijnlijk te wijten aan vierwaardig titaan dat tin vervangt.
Gemeten met: Ocean Optics Flame spectrometer, reflection/backscattering probe en een LED lichtbron van 255 nm.
Gemeten met: Ocean Optics Flame spectrometer, reflection/backscattering probe en een LED lichtbron van 255 nm.
Gemeten met: Ocean Optics Flame spectrometer, reflection/backscattering probe en een LED lichtbron van 255 nm.
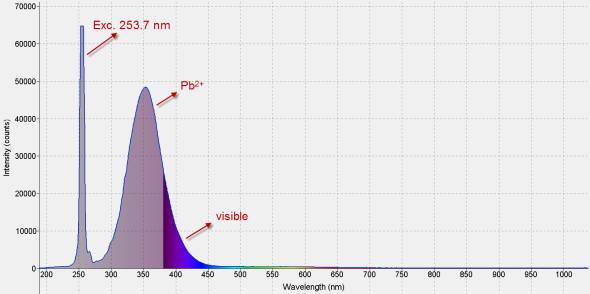
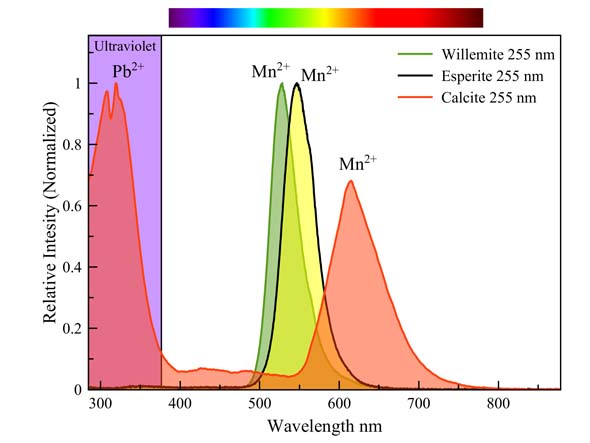
Nog geen 20 % van deze fluorescentie is zichtbaar voor het menselijk oog. Het grootste deel ervan bevindt zich in het middengebied van het UV, rond 300 nm. Lood is hier de activator.
Gemeten met: Ocean Optics Jaz spectrometer en een LED lichtbron van 255 nm.
Malayaiet
Hardystoniet
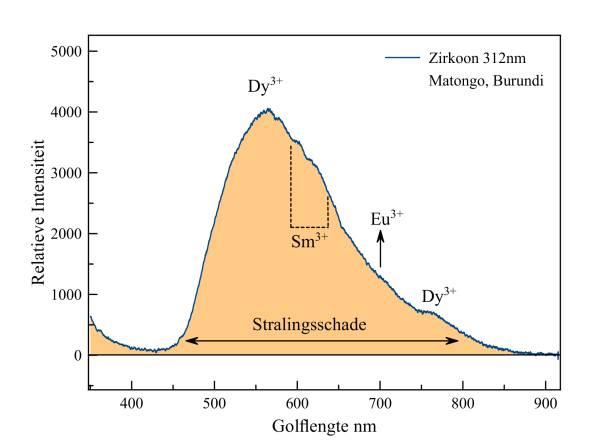
Zirkoon
De sterkste fluorescentie van zirkoon zien we onder middengebied UV. De oorzaak ligt in uitgebreide schade aan het kristalrooster door radioactief verval van isotopen van voornamelijk uraan en thorium. Bovenop de zeer brede emissiepiek van deze roosterfouten zien we emissies van samarium, europium en dysprosium, alle in driewaardige toestand.
Ernst A. J. Burke schreef een zeer interessant artikel over zirkoon uit Matongo in 1998. We publiceren het met trots en met dank aan de auteur, die ondertussen lid is van onze vereniging. U kunt de tekst als PDF downloaden door op het ikoon rechts te klikken.
Ook interessant is een artikel van A. Emmermann in Geonieuws van Januari 2010: "Zirkoon, in lichtjaren gemeten".



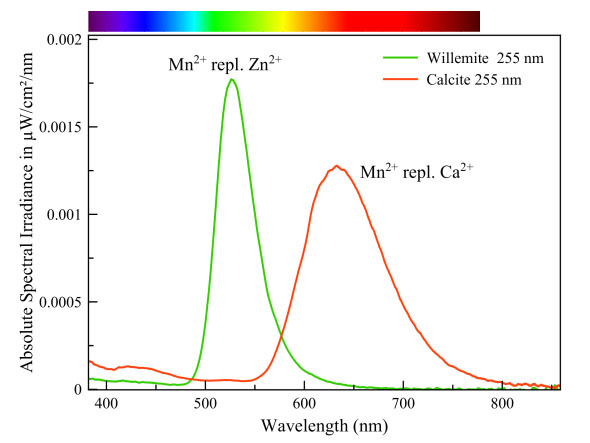
Mangaan kan een heel palet aan fluorescentiekleuren veroorzaken. De kleur hangt af van de manier waarop het mangaan-ion is ingesloten in het kristalrooster, meerbepaald van de coördinatie met de omringende zuurstofionen. Die oefenen, door hun negatieve lading, een elektrostatische druk uit op de buitenste orbitalen van het mangaanion. Die druk heeft invloed op de grootte van de energie die betrokken is bij de overgangen in het mangaan-ion. In calciet is mangaan omgeven door 6 zuurstoffen en is de transitie-energie daardoor wat kleiner dan in willemiet waar mangaan slechts door 4 zuurstoffen is ingesloten. Daardoor fluoresceert calciet rood en willemiet groen.
Willemiet & calciet
Gemeten met: Ocean Optics Flame spectrometer, reflection/backscattering probe en een LED lichtbron van 255 nm.
Gekalibreerd met de Ocean Optics HL-2000-CAL.
Calciet
Willemiet
Esperiet, Willemiet & calciet
Chroom-tremoliet - tremoliet-(Cr)
Mangaan veroorzaakt hier een verschillende fluorescentiekleur in drie mineralen die op hetzelfde specimen zitten (zie tekst bij spectrum hierboven). Het is opvallend dat het groengele esperiet slechts zeer weinig verschilt in kleur van het groene willemiet. Beide spectra overlappen voor het grootste deel. Veel mensen hebben dan ook moeite om de kleuren te onderscheiden. Mangaan heeft geen co-activator nodig in willemiet en esperiet, maar wel in calciet. Het calciet bevat enkele ppm lood, dat sterk fluoresceert in het UV tussen 280 nm en 350 nm. Dit golflengtegebied is precies geschikt voor de excitatie van mangaan in calciet.
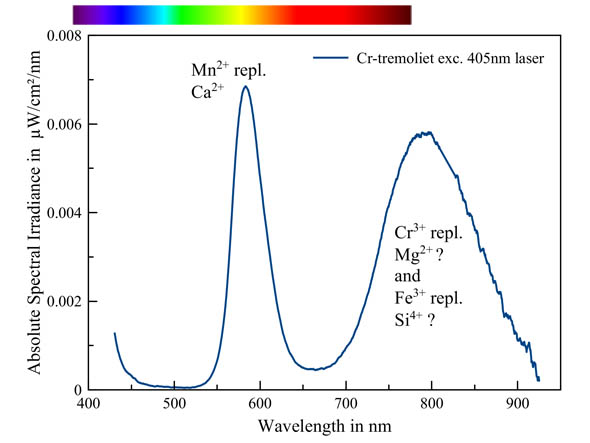
Chroom is een bekende activator die in veel mineralen een rode fluorescentie veroorzaakt. In deze tremoliet-(Cr) wordt de oranje fluorescentie echter veroorzaakt door mangaan, de meest voorkomende activator in tremoliet. Er is echter nog een sterke tweede band aanwezig in het rode en infrarode deel van het spectrum. Deze zou kunnen veroorzaakt worden door chroom dat magnesium vervangt en/of ijzer dat silicium vervangt. De literatuur blijft echter vaag daaromtrent.
Spodumeen, var. Kunziet
Spodumeen is een lithium-aluminium silikaat. Lithium is een klein ion, waardoor er niet veel elementen zijn met de geschikte afmetingen en lading om dit ion te vervangen. Silicium en de silikaatgroepen worden echter wel vrij gemakkelijk vervangen door andere elementen (en anionen) alsook aluminium.
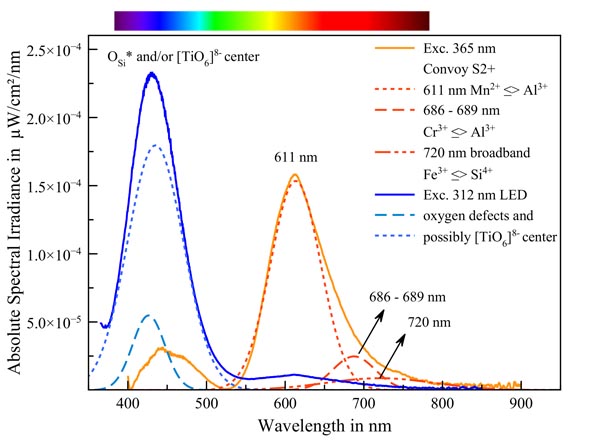
Spodumeen fluoresceert in twee kleuren naargelang de excitatie-energie. Onder de krachtige 365 nm UV-bundel van de Convoy S2+ lamp, zien we een sterke oranje emissie. Wiskundige ontleding van het spectrum in de Gaussiaanse bestanddelen levert drie duidelijke pieken op. Deze pieken vallen precies op de waarden die Gorobets en Rogojine publiceerden. (Luminescent Spectra of Minerals: Reference Book, Boris S. Gorobets & Alexandre A. Rogojine).
| Piek golflengte |
vervangen ion |
vervangend ion |
| 611 nm |
Al3+ |
Mn2+ ** |
| 686 nm - 689 nm |
Al3+ |
Cr3+ |
| 720 nm (breedband) |
Si4+ |
Fe3+ |
Vermits de oplossing van het spectrum in zijn Gaussiaansen met vrij grote nauwkeurigheid klopt met de gemeten curve (Adjusted R^2: 0.9955) kunnen we deze activators met vertrouwen puliceren.
** Gorobets vermeldt Mn2+. Andere bronnen hebben het over Mn3+, wat beter klopt qua lading.
De blauwe fluorescentie onder UV van 312 nm (het middengebied van UV) is niet met zekerheid verklaard. Gorobets heeft het over zuurstofdefecten, meerbepaald: niet doorverbonden zuurstof in de silikaatgroep. Deze defecten veroorzaken een blauwe fluorescentie in veel silikaten maar de plaats van de pieken in het spectrum klopt niet helemaal. De blauwe fluorescentie is ook wat te intens om alleen aan zuurstofdefecten toe te schrijven. Mogelijk wordt een groot deel ervan veroorzaakt door de [TiO6]8- groep die, als anion, silikaatgroepen kan vervangen. Deze [TiO6]8- groep is verantwoordelijk voor de blauwe fluorescentie van bijvoorbeeld benitoiet en dumortieriet. Gaft & al. wijzen ook in die richting maar het is nog niet grondig onderzocht.
Talk, pseudomorf na kwarts
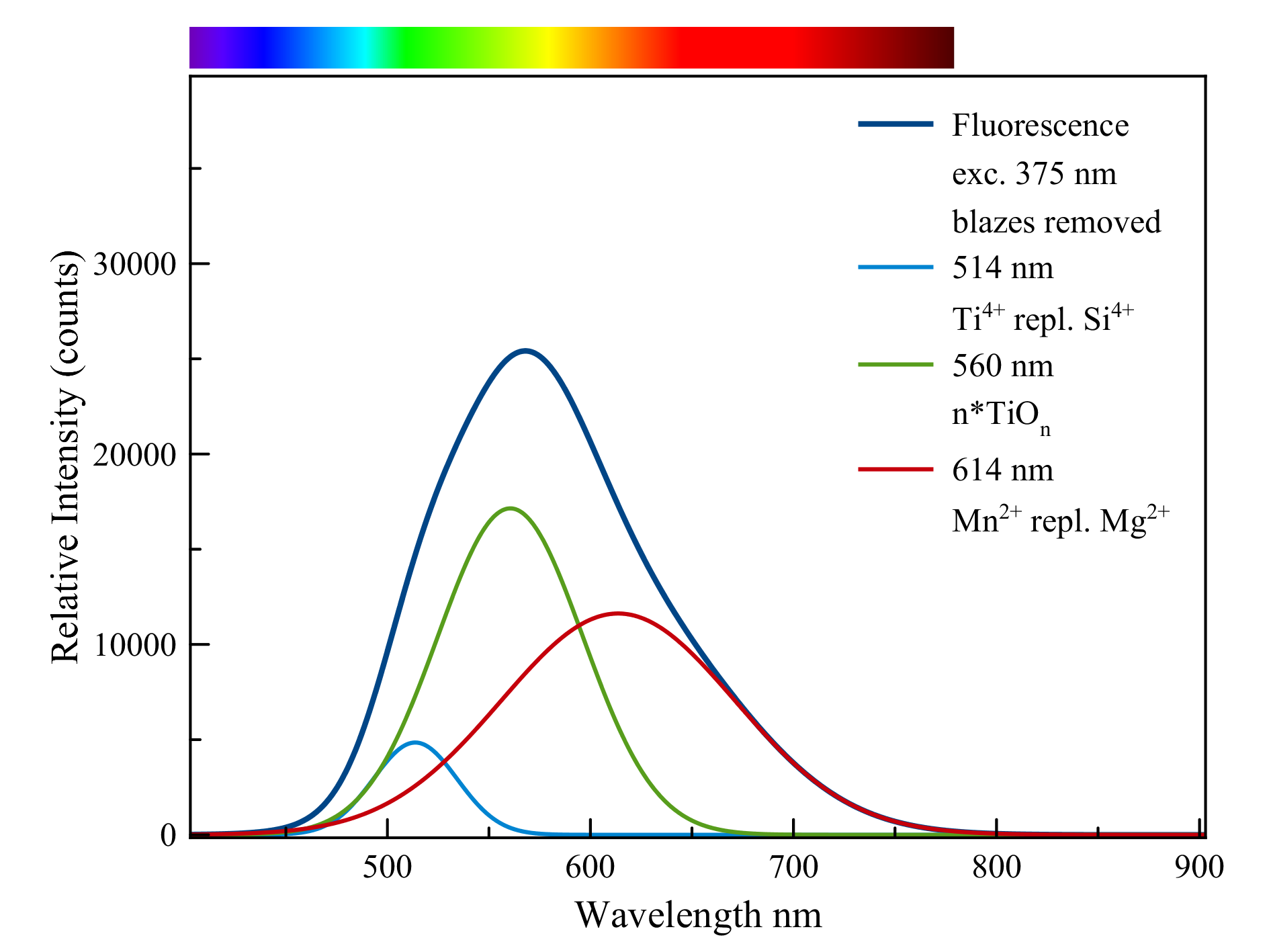
De fluorescentie van deze talk laat zich opsplitsen in drie belangrijke contibuties:
•titaan, Ti4+, als vervanger van silicium, Si4+, een groene emissie.
•clusters van het titanaat-anion, n*(TiOn)n- die in het groene en gele gebied oplichten.
•Mangaan, Mn2+, dat in talk wat magnesium vervangt met een oranje tot rode fluorescentie als gevolg.
De drie kleuren samen vormen de vuilwitte kleur die op de ribben van de kristallen zichtbaar is. De kristalvlakken zelf fluoresceren, zo lijkt het althans, een zwak bruin. Dat is echter het gevolg van het vuilwitte licht dat gefilterd wordt door de roestbruine oppervlaktelaag. De fluorescentie is zwak tot zeer zwak onder normale UV-lampen maar veel sterker onder het licht van de Convoy S2+ LED-lamp

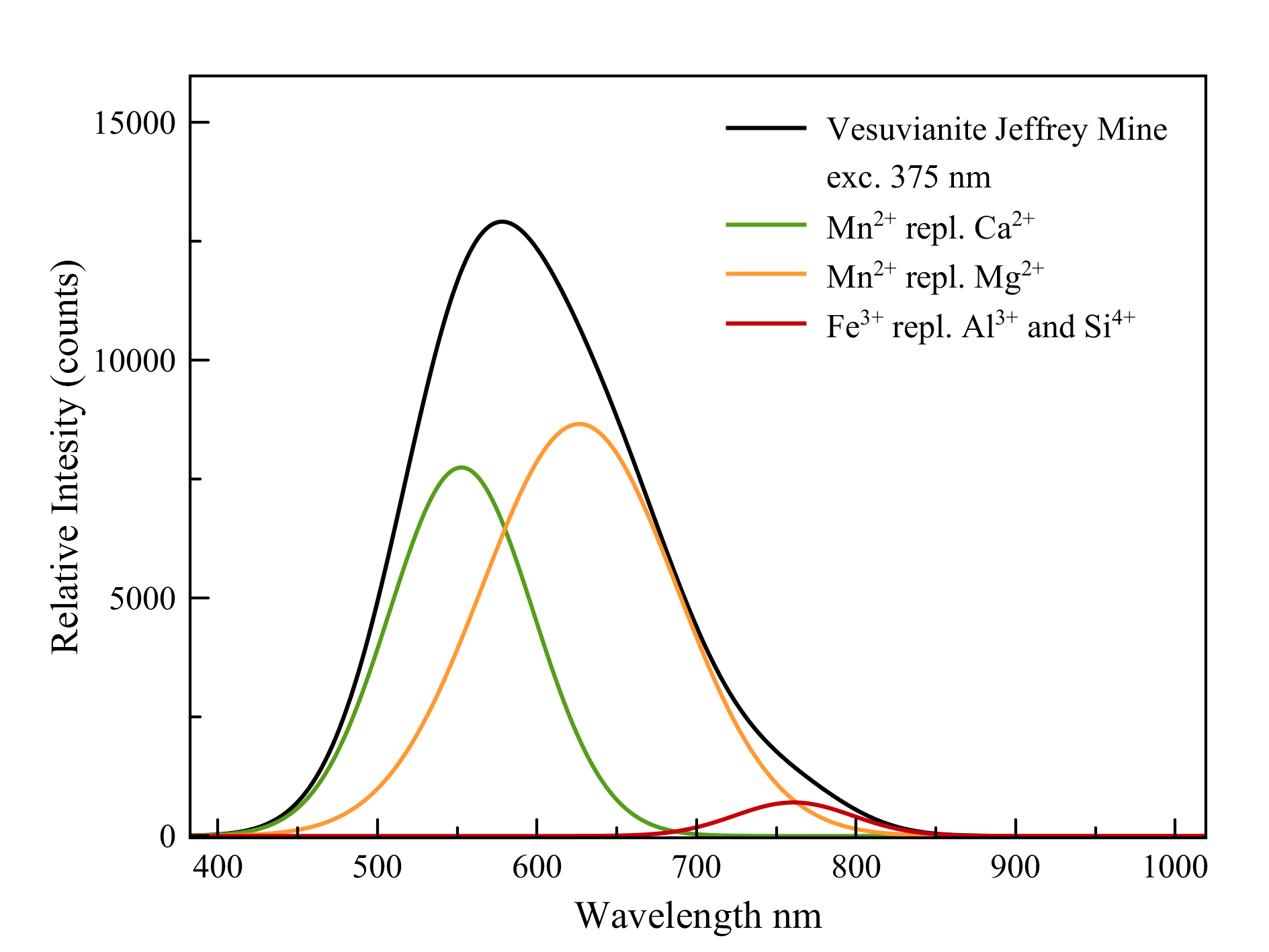
Vesuvianiet
Ca10Mg2Al4(SiO4)5(Si2O7)2(OH)4
Zoals blijkt uit de formule bevat vesuvianiet twee ion die door mangaan kunnen vervangen worden: calcium en magnesium. De sites waarin deze ionen zitten zijn lichtjes verschillend qua afmetingen en omgeving. Als gevolg zal mangaan in deze sites ook lichtjes verschillend fluoresceren. Beide emissies overlappen elkaar wel en zorgen voor een brede piek. Er is ook wat driewaardig ijzer aanwezig dat graag aluminium en zelfs, in mindere mate, silicium vervangt. Daaruit ontstaat dan weer een dieprode fluorescentie.